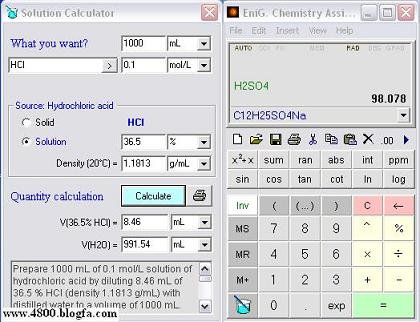
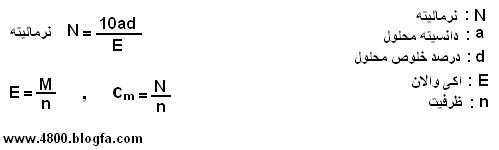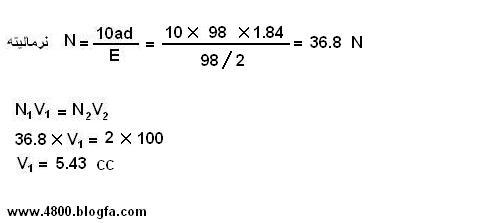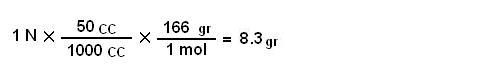با تشکر از دوست عزیز که این طمالب را در تاپیک نرم افزارهای شیمی قرار داده بود به دیل جامع تر شدن تاپیک مجددا اینجا قرار میدهم
[FONT=Tahoma, Arial, Helvetica, sans-serif]محلول سازی[/FONT]
[FONT=Tahoma, Arial, Helvetica, sans-serif]محلول سازی یکی از ابتدایی ترین کارهای در ازمایشگاه است که لازمه هر کار ازمایشگاهی است به همین جهت در این جا روش های ساده ومختصری در مورد محلول سازی در ازمایشگاه برای شما جمع اوری کرده ام و امیدوارم که مورد استفاده قرار گیرد.[/FONT]
[FONT=Tahoma, Arial, Helvetica, sans-serif]محلول سازی از محلول های غلیظ ازمایشگاه[/FONT]
[FONT=Tahoma, Arial, Helvetica, sans-serif]معمولا در ازمایشگاه محلول ها به صورت غلیظ و با درصد خلوص مشخص و استانداردی وجود دارد و برای تهیه محلول های رقیق تر باید از ان ها استفاده کرد.[/FONT]
[FONT=Tahoma, Arial, Helvetica, sans-serif]برای این کار از روابط رقیق سازی استفاده می کنیم :[/FONT]
[FONT=Tahoma, Arial, Helvetica, sans-serif]
[/FONT]
[FONT=Tahoma, Arial, Helvetica, sans-serif]در رابطه بالا نیاز است که نرمالیته یا مولاریته محلول غلیظ موجود در ازمایشگاه را تعیین کنیم. برای تعیین نرمالیته از فرمول زیر استفاده می کنیم :[/FONT]
[FONT=Tahoma, Arial, Helvetica, sans-serif]
[FONT=Tahoma, Arial, Helvetica, sans-serif]نرمالیته محلول غلیظ را بدست اوردیم. در رابطه اول فقط حجم محلول غلیظ ( v2 ) مجهول است که محاسبه می شود و فقط کافی است این مقدار (v1)را از محلول غلیظ برداشته و به حجم مورد نظر ( v2 ) برسانیم.[/FONT][/FONT]
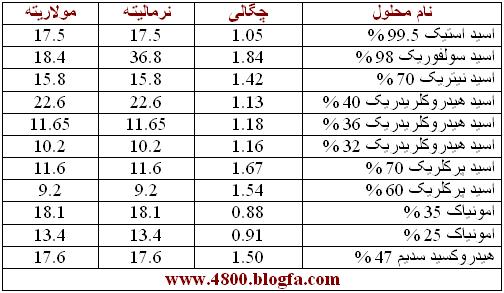
[FONT=Tahoma, Arial, Helvetica, sans-serif]برای تعیین نرمالیته و مولاریته محلول های ازمایشگاهی می توانید از جدول زیر استفاده کنید. که در این صورت فقط به رابطه اول نیاز خواهید داشت. [/FONT]
[FONT=Tahoma, Arial, Helvetica, sans-serif]مثال :[/FONT]
[FONT=Tahoma, Arial, Helvetica, sans-serif]100cc محلول اسید سولفوریک 2N تهیه کنید ؟
[FONT=Tahoma, Arial, Helvetica, sans-serif]اطلاعاتی نظیر دانسیته , درصد خلوص , جرم مولکولی و ... را می توانید از برچسب روی ظرف محلول بدست اورید.
[/FONT][/FONT] [FONT=Tahoma, Arial, Helvetica, sans-serif]مقدار 5.43cc از محلول غلیظ اسید سولفوریک برداشته و به حجم 100cc برسانید. ( در بالون ژوژه 100cc )[/FONT]
[FONT=Tahoma, Arial, Helvetica, sans-serif]تذکر : در مورد اسید های غلیظ و قوی مثل اسید سولفوریک همیشه اسید را به اب اضافه می کنیم. ( قبل از اضافه کردن اسید مقداری اب مقطر در بالون بریزید و سپس اسید را اضافه کنید. )[/FONT]
[FONT=Tahoma, Arial, Helvetica, sans-serif]محلول سازی از مواد جامد ازمایشگاه[/FONT]
[FONT=Tahoma, Arial, Helvetica, sans-serif]برای محلول سازی از مواد جامد ازمایشگاه از رابطه زیر استفاده کنید :[/FONT]
[FONT=Tahoma, Arial, Helvetica, sans-serif]فقط کافی است مقدار ماده جامد بدست امده را در مقداری اب مقطر حل کرده و به حجم مورد نظر برسانید.[/FONT]
[FONT=Tahoma, Arial, Helvetica, sans-serif]مثال :[/FONT]
[FONT=Tahoma, Arial, Helvetica, sans-serif]50cc محلول یک نرمال یدید پتاسیم تهیه کنید؟[/FONT]
[FONT=Tahoma, Arial, Helvetica, sans-serif](جرم مولکولی یدید پتاسیم : 166grگرم )[/FONT]
[FONT=Tahoma, Arial, Helvetica, sans-serif]اگر دقیقا ۸.3gr از یدید پتاسیم را در 50cc اب مقطر حل کنیم محلول یک نرمال بدست خواهد امد.[/FONT]
تذکر : در مورد برخی مواد جامد که رطوبت جذب می کنند باید دقت شود که از فرمول نوشته شده بر روی برچسب ظرف ماده جرم مولکولی محاسبه شود . مثلا BaCl2 . 2H2O به جرم مولکولی ان دو ملکول اب ( 36gr ) اضافه شده است که باید در محاسبات لحاظ شود.
[FONT=Tahoma, Arial, Helvetica, sans-serif]تهیه چند محلول دیگر :[/FONT]
[FONT=Tahoma, Arial, Helvetica, sans-serif]100cc محلول استات سدیم 10% ( وزنی - حجمی ) تهیه کنید؟[/FONT]
[FONT=Tahoma, Arial, Helvetica, sans-serif]استات سدیم جامد است و در مورد جامدات فقط کافی است مقدار 10 گرم استات سرب را وزن کرده و به حجم 100cc برسانید.(واضح است که اگر 200ccمحلول بخواهیم باید 20gr گرم را در 200cc حل کنیم.)[/FONT]
[FONT=tahoma,verdana,arial,helvetica,sans-serif]نکته : در مورد مایعات حجم مربوط باید کم شود . در مورد جامدات به دلیل حل شدن ذرات جامد در بین حلال و نداشتن تاثیر ان چنان در تغییر حجم می توان از حجم ماده جامد صرفه نظر کرد اما مایعات این چنین نیست ( 10 سی سی محلول مورد نظر و 90 سی سی اب مقطر برای 10% حجمی - حجمی )[/FONT]
[FONT=Tahoma, Arial, Helvetica, sans-serif]محلول 2:1 ( دو به یک ) اتانول تهیه کنید؟[/FONT]
[FONT=Tahoma, Arial, Helvetica, sans-serif]یعنی به ازای یک سی سی اتانول دو سی سی اب مقطر اضافه کنید.[/FONT]
۱۰۰cc محلول اسید کلریدریک %25 از اسید کلریدریک غیظ %37 بسازید.
برای این کار طبق روش زیر محاسبه کنید و به اندازه مقدار بدست امده از محلول غلیظ برداشته و با اب مقطر به حجم مورد نظر برسانید.
مقدار 67.5cc از اسید کلریدریک %37 برداشته و در یک بالون 100cc با اب مقطر به حجم برسانید.
به نقل از: http://4800.blogfa.com/post-59.aspx
=========================================