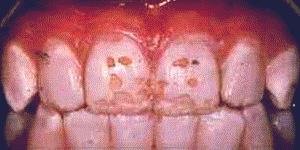
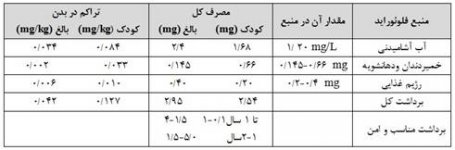
این مقاله به بررسی تركیبات موجود در آب آشامیدنی بالاخص فلوراید می پردازد، همانگونه كه مسلم است آب مهمترین مایحتاج بشر برای زندگی میباشد .پس پرواضح است كه شناخت آب می تواند كمك شایانی به ما در رابطه با استفاده بهینه از این مایع حیات بخش نماید همچنین با بررسی تركیبات موجود در آب می توانیم از رسیدن صدمات احتمالی ناشی از مصرف آب آلوده جلوگیری نماییم .با توجه به اینكه املاح و مواد گوناگونی در آب وجود دارند و برخی از آنها برای سلامتی مضر است لذا سعی شده است مقدار مجاز برخی از آنها با توجه به استانداردهای جهانی ارائه گردد تا بدین وسیله به روشنگری در این خصوص پرداخته باشیم.البته نكته قابل توجه این است كه این مقاله بصورت (part to part) نگاشته شده است تا بصورت واقعی ارائه شود و هیچگونه تغییری در متن اصلی داده نشود ، در ادامه نیز نگاهی گذرا به آب برخی مناطق و تركیبات موجود در آنها خواهیم داشت جهت تهیه این مقاله از سایتهای مختلف اینترنتی و همچنین منابع فارسی استفاده شده است كه در انتهای مقاله در قسمت مراجع به آنها پرداخته شده است .
مقدمه
آبی كه ما می نوشیم حاوی املاح و مواد گوناگونی می باشد كه پاره ای از آنها مضر و پاره ای دیگر نه تنها مضر نیستند بلكه برای سوخت وساز بدن بسیار مفید می باشند . مواد موجود در آب را می توان به شاخه های بیولوژیكی كه عبارتند از انواع میكروبها و ویروسهاوانگلها و آمیب ها و ... ،و شیمیائی كه عبارتست از عناصر ومواد شیمیائی نظیر بی كربنات وانواع كاتیونها آنیونها كربناتها سولفاتها فسفاتها و ... كه وجود برخی از آنها در آب مایه سلامت و برخی دیگر عامل نقاهت و مرض می باشد .آب یكی از مهمترین و پر قدرت ترین حلالهای شیمیایی می باشد لذا آب جاری با توجه به تركیبات شیمیایی بسترخود مقداری از عناصر را در خود حل می كند در زیر به بررسی اجمالی آنها می پردازیم.تركیبات موجود درآب عبارتنداز : نیترات ونیتریت ، آهن و منگنز، جامدات معلق،سولفات ، فسفات ،كلراید، فلوراید ،كلسیم و سدیم وعناصرناچیز
▪ درصد فراوانی عناصر در پوسته زمین:
جامدات معلق جامداتی هستند كه محلول حقیقی نبوده و می توان با صاف كردن از محیط حذفشان نمود . جامدات كل معرف مجموع جامدات حل شده وجامدات معلق می باشد (اكثر اوقات به مقدار جامدات كل مانده كل هم اطلاق می شود . در آب با منشأ، بستری است كه آب در آن جاری می باشد از عوامل دیگر ایجاد مواد معلق می توان به نقش كارخانجات صنعتی و كارگاهها كودهای كشاورزی فاضلابهای شهری وصنعتی وكشاورزی و.... در ایجاد مواد معلق اشاره نمود .استانداردهای سازمان بهداشت آب آشامیدنی آمریكا مقدار كل جامدات را برای یك آب قابل شرب خوب(۵۰۰ ppm) خاطر نشان كرده است اما اگر در ایالتی و یا ناحیه ای نتوان به این استاندارد دست یافت مقدار(۱۰۰۰ppm ) نیز اجازه داده شده است .لازم به ذكر است كه عملاً هیچ محدودیتی بطور مستقیم بر روی مقدار جامدات حل شده و معلق اعمال نگردیده و این محدوده توسط كدورت آب كه نباید از (۱۰) واحد تجاوز كندكنترل می شود .
نیترات
نیتریت ونیترات از دیگر مواد موجود درآب می باشند كه معمولاً به مقدار نسبتاً كمی در آبهای طبیعی یافت می شوند ، احتمالاً تركیبات نیتروژن دار از طریق فاضلاب های صنعتی و كشاورزی وتاحدودی صنعتی به این آبها وارد می شوند كه با اكسید شدن این تركیبات به نیترات توأم است، اداره بهداشت ایالات متحده آمریكا در ارتباط با استانداردهای آب آشامیدنی ،هیچگونه محدودیتی را در ارتباط با مقدار محتوی نیترات در آب عمل نكرده است . اخیراً،مشخص شده كه وجود غلضت های بالایی از نیترات بالای ppm ۱۰ ? دلیل آبی شدن رنگ نوزادان تحت عنوان methem eglobinemia می باشد معمولاً وجود چنین غلظت های بالایی مربوط به آب چاههایی در مناطق روستایی و نزدیك به منابع نفوذ سطحی می باشد.(البته این تحقیق مربوط به كشور آمریكا می باشد).
آهن
آهن به دو گونه آهن فرو و آهن فریك وجود دارد . آهن در فرم فریك كاملاً اكسیده شده در حالیكه در وضعیت فرو ، به گونه ای جزئی اكسیده می گردد . در آزمایش مقدار كل محلول شده و دو نوع ، یعنی آهن فرو و آهن فریك مورد سنجش قرار می گیرد . از آنجاییكه آهن یكی از فراوانترین عناصر پوسته جامد زمین می باشد در اكثر آبهای طبیعی وجود دارد .آهن در آبهای سطحی به دلیل اكسید شدن توسط اكسیژن ، به صورت فریك می باشد ، اما آهن در آبهای چاه ، معمولاً بصورت فرو دیده می شود ، وقتی آب از درون چاه به سطح زمبن آورده می شود ،به محض تماس با هوای بیرون گاز دی اكسید كربن آزاد گشته و آهن فرو تبدیل به آهن فریك می گردد .آهن در رده عناصر قشر ساز شبیه كلسیم و منیزیم قرار داده شده است و دلیل آنهم تشكیل رسوب از محلول و تولید یك لایه می باشد ، آهن در آب اشكالات زیادی را تولید می كند ، تولید لكه هایی میكند كه لایه حفاظتی و بهداشتی دستشوئی ها را از بین برده و بر سایر ظروف مشابه تأثیرات سوئی می گذارد . از نقطه نظر قوانین بهداشتی دولت ایالات متحده آمریكا ،حداكثر مقدار این ماده دردرون آب قابل شرب حدود ۰.۳ ppm بصورتFeاست. (۲) (۳) از آنجا كه حضور آهن به مقدار فراوان باعث ناهنجاریهای بهداشتی می گردد از اینرو حذف آن بسیار حائز اهمیت می باشد .
▪ حذف آهن از محیط به همراه فرآیندهای زیر صورت می گیرد
منگنز بیشتر در آبهای آهن دار با دامنه ای كمتر از آهن وجود دارد. اشكالاتی كه در اثر حضور هریك از آنان بوجود می آید شبیه یكدیگر می باشد وروش حذف آهن بر منگنز نیز تأثیر می گذارد . منگنز بیشتر در آبها وجود داشته و معمولاً مقدارش بیشتر از ۳ ppm نمی باشد این عنصر ،مانندآهن از محلول راسب می شود و به فرم هیدروكسید منگنز قهوه ای یا سیاه رنگ در درون لوله های انتقال ، شیرها و غیره دیده می شود حضور منگنز تولید یكسری لكه های بد رنگ می كند . مقدار منگنز برای اكثر اهداف صنعتی نبایستی بیشتر از(0.1 ppm ۴) باشد و جهت تعدادی از فرایندها ، مانند تولید كاغذهای نرم و نازك ، این مقدار منگنز هم به عنوان آلوده كننده مطرح می شود .استاندارد اداره بهداشت آمریكا در این مورد بیشتر نبودن منگنز بصورت Mn درحدود 0.5 ppm ? در آب آشامیدنی را توصیه می نماید .
مقدمه
آبی كه ما می نوشیم حاوی املاح و مواد گوناگونی می باشد كه پاره ای از آنها مضر و پاره ای دیگر نه تنها مضر نیستند بلكه برای سوخت وساز بدن بسیار مفید می باشند . مواد موجود در آب را می توان به شاخه های بیولوژیكی كه عبارتند از انواع میكروبها و ویروسهاوانگلها و آمیب ها و ... ،و شیمیائی كه عبارتست از عناصر ومواد شیمیائی نظیر بی كربنات وانواع كاتیونها آنیونها كربناتها سولفاتها فسفاتها و ... كه وجود برخی از آنها در آب مایه سلامت و برخی دیگر عامل نقاهت و مرض می باشد .آب یكی از مهمترین و پر قدرت ترین حلالهای شیمیایی می باشد لذا آب جاری با توجه به تركیبات شیمیایی بسترخود مقداری از عناصر را در خود حل می كند در زیر به بررسی اجمالی آنها می پردازیم.تركیبات موجود درآب عبارتنداز : نیترات ونیتریت ، آهن و منگنز، جامدات معلق،سولفات ، فسفات ،كلراید، فلوراید ،كلسیم و سدیم وعناصرناچیز
▪ درصد فراوانی عناصر در پوسته زمین:
ـ اكسیژن ۴۹.۵% سدیم ۲.۶۳% كلر 0.1۹% باریم ۰.۰۴%
ـ سیلیسیم ۲۵.۷% پتاسیم ۲.۴۰% فسفر 0.1۱% نیتروژن ۰.۰۳%
- آلومینیم ۷.۴% منیزیم ۱.۹۳% منگنز ۰.۰۹% فلوئور ۰.۰۳%
ـ آهن ۴.۷% هیدروژن ۰.۹% كربن ۰.۰۸% استرانسیم ۰.۰۲%
ـ كلسیم ۳.۴% تیتانیوم ۰.۶% گوگرد ۰.۰۶% سایر عناصر ۰.۴۷%
جامدات معلقـ سیلیسیم ۲۵.۷% پتاسیم ۲.۴۰% فسفر 0.1۱% نیتروژن ۰.۰۳%
- آلومینیم ۷.۴% منیزیم ۱.۹۳% منگنز ۰.۰۹% فلوئور ۰.۰۳%
ـ آهن ۴.۷% هیدروژن ۰.۹% كربن ۰.۰۸% استرانسیم ۰.۰۲%
ـ كلسیم ۳.۴% تیتانیوم ۰.۶% گوگرد ۰.۰۶% سایر عناصر ۰.۴۷%
جامدات معلق جامداتی هستند كه محلول حقیقی نبوده و می توان با صاف كردن از محیط حذفشان نمود . جامدات كل معرف مجموع جامدات حل شده وجامدات معلق می باشد (اكثر اوقات به مقدار جامدات كل مانده كل هم اطلاق می شود . در آب با منشأ، بستری است كه آب در آن جاری می باشد از عوامل دیگر ایجاد مواد معلق می توان به نقش كارخانجات صنعتی و كارگاهها كودهای كشاورزی فاضلابهای شهری وصنعتی وكشاورزی و.... در ایجاد مواد معلق اشاره نمود .استانداردهای سازمان بهداشت آب آشامیدنی آمریكا مقدار كل جامدات را برای یك آب قابل شرب خوب(۵۰۰ ppm) خاطر نشان كرده است اما اگر در ایالتی و یا ناحیه ای نتوان به این استاندارد دست یافت مقدار(۱۰۰۰ppm ) نیز اجازه داده شده است .لازم به ذكر است كه عملاً هیچ محدودیتی بطور مستقیم بر روی مقدار جامدات حل شده و معلق اعمال نگردیده و این محدوده توسط كدورت آب كه نباید از (۱۰) واحد تجاوز كندكنترل می شود .
نیترات
نیتریت ونیترات از دیگر مواد موجود درآب می باشند كه معمولاً به مقدار نسبتاً كمی در آبهای طبیعی یافت می شوند ، احتمالاً تركیبات نیتروژن دار از طریق فاضلاب های صنعتی و كشاورزی وتاحدودی صنعتی به این آبها وارد می شوند كه با اكسید شدن این تركیبات به نیترات توأم است، اداره بهداشت ایالات متحده آمریكا در ارتباط با استانداردهای آب آشامیدنی ،هیچگونه محدودیتی را در ارتباط با مقدار محتوی نیترات در آب عمل نكرده است . اخیراً،مشخص شده كه وجود غلضت های بالایی از نیترات بالای ppm ۱۰ ? دلیل آبی شدن رنگ نوزادان تحت عنوان methem eglobinemia می باشد معمولاً وجود چنین غلظت های بالایی مربوط به آب چاههایی در مناطق روستایی و نزدیك به منابع نفوذ سطحی می باشد.(البته این تحقیق مربوط به كشور آمریكا می باشد).
آهن
آهن به دو گونه آهن فرو و آهن فریك وجود دارد . آهن در فرم فریك كاملاً اكسیده شده در حالیكه در وضعیت فرو ، به گونه ای جزئی اكسیده می گردد . در آزمایش مقدار كل محلول شده و دو نوع ، یعنی آهن فرو و آهن فریك مورد سنجش قرار می گیرد . از آنجاییكه آهن یكی از فراوانترین عناصر پوسته جامد زمین می باشد در اكثر آبهای طبیعی وجود دارد .آهن در آبهای سطحی به دلیل اكسید شدن توسط اكسیژن ، به صورت فریك می باشد ، اما آهن در آبهای چاه ، معمولاً بصورت فرو دیده می شود ، وقتی آب از درون چاه به سطح زمبن آورده می شود ،به محض تماس با هوای بیرون گاز دی اكسید كربن آزاد گشته و آهن فرو تبدیل به آهن فریك می گردد .آهن در رده عناصر قشر ساز شبیه كلسیم و منیزیم قرار داده شده است و دلیل آنهم تشكیل رسوب از محلول و تولید یك لایه می باشد ، آهن در آب اشكالات زیادی را تولید می كند ، تولید لكه هایی میكند كه لایه حفاظتی و بهداشتی دستشوئی ها را از بین برده و بر سایر ظروف مشابه تأثیرات سوئی می گذارد . از نقطه نظر قوانین بهداشتی دولت ایالات متحده آمریكا ،حداكثر مقدار این ماده دردرون آب قابل شرب حدود ۰.۳ ppm بصورتFeاست. (۲) (۳) از آنجا كه حضور آهن به مقدار فراوان باعث ناهنجاریهای بهداشتی می گردد از اینرو حذف آن بسیار حائز اهمیت می باشد .
▪ حذف آهن از محیط به همراه فرآیندهای زیر صورت می گیرد
۱) هوا دادن
۲) منعقد ساختن
۳) نرم كردن توسط آهك و آهك كربنات سدیم
۴) تبادل یونی
۵) صافسازی تماسی
منگنز۲) منعقد ساختن
۳) نرم كردن توسط آهك و آهك كربنات سدیم
۴) تبادل یونی
۵) صافسازی تماسی
منگنز بیشتر در آبهای آهن دار با دامنه ای كمتر از آهن وجود دارد. اشكالاتی كه در اثر حضور هریك از آنان بوجود می آید شبیه یكدیگر می باشد وروش حذف آهن بر منگنز نیز تأثیر می گذارد . منگنز بیشتر در آبها وجود داشته و معمولاً مقدارش بیشتر از ۳ ppm نمی باشد این عنصر ،مانندآهن از محلول راسب می شود و به فرم هیدروكسید منگنز قهوه ای یا سیاه رنگ در درون لوله های انتقال ، شیرها و غیره دیده می شود حضور منگنز تولید یكسری لكه های بد رنگ می كند . مقدار منگنز برای اكثر اهداف صنعتی نبایستی بیشتر از(0.1 ppm ۴) باشد و جهت تعدادی از فرایندها ، مانند تولید كاغذهای نرم و نازك ، این مقدار منگنز هم به عنوان آلوده كننده مطرح می شود .استاندارد اداره بهداشت آمریكا در این مورد بیشتر نبودن منگنز بصورت Mn درحدود 0.5 ppm ? در آب آشامیدنی را توصیه می نماید .
آخرین ویرایش توسط مدیر: