You are using an out of date browser. It may not display this or other websites correctly.
You should upgrade or use an alternative browser.
You should upgrade or use an alternative browser.
جدول تناوبی
- شروع کننده موضوع MOJTABA 77
- تاریخ شروع
تغییر تاریخی در جدول تناوبی عناصر
تغییر تاریخی در جدول تناوبی عناصر
تغییر تاریخی در جدول تناوبی عناصر
جدول تناوبی عناصر را حفظ کرده اید؟ برای خیلی از ما خواندن و حفظ کردن جدولی که آقای مندلیف پایه گذارش بوده بخشی از خاطرات دوران مدرسه را تشکیل می دهد.
با کشفیات جدید، شیمیدان ها می گویند این جدول دچار تغییرات مهمی شده است. به گونه ای که آن را یک تغییر تاریخی نامیده اند. آنها متوجه شده اند که "جرم اتمی" ده عنصر این جدول باید تغییر کند. تا به حال برای این عناصر یک جرم اتمی ثابت در نظر گرفته میشد. اما مطالعات جدید نشان می دهد این عناصر بسته به اینکه از کجا استخراج شده باشند، جرم اتمی متفاوتی دارند.
دانشمندان متوجه شده اند که جرم اتمی هیدروژن، لیتیوم، برم، کربن، نیتروژن، اکسیژن، سیلیس، گوگرد، کلر و تالیوم بسته به اینکه از کجا به دست بیایند متفاوت است.
مقرر شده که جدول تناوبی عناصر بر اساس کشف جدید تغییر پیدا کند و قرار است این تغییر در سال ۲۰۱۱ میلادی انجام پذیرد.
با کشفیات جدید، شیمیدان ها می گویند این جدول دچار تغییرات مهمی شده است. به گونه ای که آن را یک تغییر تاریخی نامیده اند. آنها متوجه شده اند که "جرم اتمی" ده عنصر این جدول باید تغییر کند. تا به حال برای این عناصر یک جرم اتمی ثابت در نظر گرفته میشد. اما مطالعات جدید نشان می دهد این عناصر بسته به اینکه از کجا استخراج شده باشند، جرم اتمی متفاوتی دارند.
دانشمندان متوجه شده اند که جرم اتمی هیدروژن، لیتیوم، برم، کربن، نیتروژن، اکسیژن، سیلیس، گوگرد، کلر و تالیوم بسته به اینکه از کجا به دست بیایند متفاوت است.
مقرر شده که جدول تناوبی عناصر بر اساس کشف جدید تغییر پیدا کند و قرار است این تغییر در سال ۲۰۱۱ میلادی انجام پذیرد.
منبع
یادگیری جدول تناوبی
یادگیری جدول تناوبی
اما اول از همه جدول تناوبی:
جدول تناوبی عناصر شیمیایی نمایشی از عناصر شیمیایی است که براساس ساختار الکترونی مرتب شده است، بطوریکه بسیاری از خواص شیمیایی بصورت منظم در طول جدول تغییر نماید. جدول اولیه بدون اطلاع از ساختار داخلی اتمها ساخته شد: اگر عناصر را بر حسب جرم اتمی آنها مرتب نمائیم، و آنگاه نمودار خواص معین دیگر آنها را بر حسب جرم اتمی رسم نمائیم، میتوان نوسان یا تناوب این خواص را بصورت تابعی از جرم اتمی مشاهده نمود. اولین کسی که توانست این نظم را مشاهده نماید، یک شیمیدان آلمانی به نام Johann Wolfgang D?einer بود. او متوجه تعدادی تثلیث از عناصر مشابه شد:
نمونه تثلیث ها
عنصر جرم اتمی چگالی ------ عنصر جرم اتمی چگالی
Cl 35.5 1.56 g/L ------ Ca 40.1 1.55 g/cm3
Br 79.9 3.12 g/L ------ Sr 87.6 2.6 g/cm3
I 126.9 4.95 g/L ------ Ba 137 3.5 g/cm3
و به دنبال او، شیمیدان انگلیسی John Alexander Reina Newlands متوجه گردید که عناصر از نوع مشابه در فاصلههای هشت تایی یافت می شوند، که آنها را با نتهای هشتگانه موسیقی شبیه نمود، هرچند که قانون نتهای او مورد تمسخر معاصرین او قرار گرفت. سرانجام شیمیدان آلمانی Lothar Meyer و شیمیدان روسی Dmitry Ivanovich Mendeleev تقریبا بطور همزمان اولین جدول تناوبی را، با مرتب نمودن عناصر بر حسب جرمشان، توسعه دادند( ولی مندلیف تعداد کمی از عناصر را خارج از ترتیب صریح جرمی، برای تطابق بهتر با خواص همسایگانشان رسم نمود – این کار بعدها با کشف ساختار الکترونی عناصر در اواخر قرن نوزدهم و اوایل قرن بیستم توجیه گردید). فهرست عناصر بر اساس نام، علامت اختصاری و عدد اتمی موجود میباشد. شکل زیر جدول تناوبی عناصر شناخته شده را نمایش میدهد. هر عنصر با عدد اتمی و علامتهای شیمیایی. عناصر در یک ستون ("گروه") از لحاظ شیمیایی مشابه می باشند.
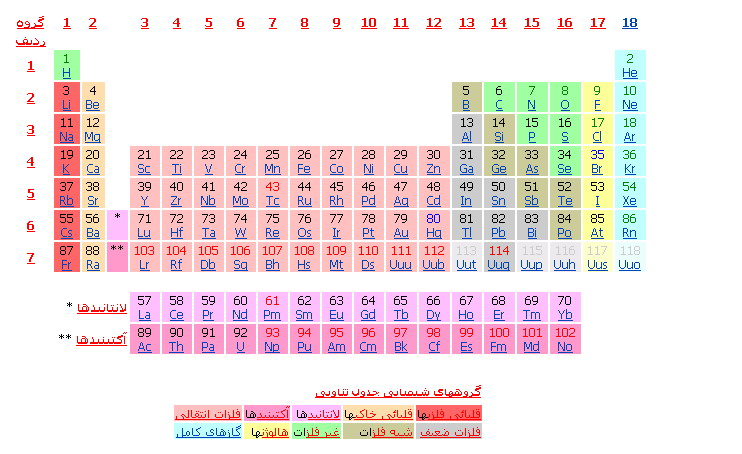
کد رنگ برای اعداد اتمی:
عناصر شماره گذاری شده با رنگ آبی ، در دمای اتاق مایع هستند؛
عناصر شماره گذاری شده با رنگ سبز ، در دمای اتاق بصورت گاز می باشند؛
عناصر شماره گذاری شده با رنگ سیاه، در دمای اتاق جامد هستند.
عناصر شماره گذاری شده با رنگ قرمز ترکیبی بوده و بطور طبیعی یافت نمی شوند(همه در دمای اتاق جامد هستند.)
عناصر شماره گذاری شده با رنگ خاکستری ، هنوز کشف نشدهاند (و بصورت کم رنگ نشان داده شدهاند تا گروه شیمیایی را که در آن قرار می گیرند، مشخص نماید.(
و می توانید دراین کلید واژه جدول برای تشدید مغناطیسی را بیابید.
تعداد لایه الکترون در یک اتم تعیین کننده ردیفی است که در آن قرار می گیرد. هر لایه به زیرلایه های متفاوتی تقسیم میشود، که هر اندازه عدد اتمی افزایش می یابد، این لایه ها به ترتیب زیر:
1s
2s 2p
3s 3p
4s 3d 4p
5s 4d 5p
6s 4f 5d 6p
7s 5f 6d 7p
8s 5g 6f 7d 8p
...
براساس ساختار جدول پر میشوند. از آنجائیکه الکترونهای خارجی ترین لایه، خواص شیمیایی را تعیین مینمایند، این لایه ها در میان گروهای یکسان مشابه اند.عناصر همجوار با یکدیگر در یک گروه، علیرغم اختلاف مهم در جرم، دارای خواص فیزیکی مشابه میباشند. عناصر همجوار با یکدیگر در یک ردیف دارای جرم های مشابه ولی خواص متفاوت میباشند.
برای مثال، عناصر بسیار نزدیک به نیتروژن (N) در ردیف دوم کربن© و اکسیژن(O) میباشند. علیرغم تشابه آنها در جرم ( که بصورت ناچیزی در واحد جرم اتمی تفاوت دارند)، دارای خواص بینهایت متفاوتی هستند، همانطور که با بررسی فرمهای دیگر میتوان ملاحظه نمود: اکسیژن دو اتمی یک کاز است که سوختن را تشدید می نماید، نیتروژن دو اتمی یک گاز است که سوختن را تشدید نمی کند، و کربن یک جامد است که میتواند سوزانده شود( بله، میتوان الماس را سوزاند!).
در مقایسه، عناصر بسیار نزدیک به کلر (Cl) در گروه یکی مانده به آخر در جدول «هالوژنها) فلوئور( F) و برم( Br) میباشند. علیرغم تفاوت فاحش جرم آنها در گروه، فرمهای دیگر آنها دارای خواص بسیار مشابه میباشند: آنها بسیار خورنده ( بدین معنی که تمایل خوبی برای ترکیب با فلزات، برای تشکیل نمک هالاید فلز)؛ کلر و فلوئور گاز هستند، درحالیکه برم یک مایع با تبخیر بسیار کم میباشد؛ کلر و برم بسیار رنگی هستند
یادگیری جدول تناوبی
اما اول از همه جدول تناوبی:
جدول تناوبی عناصر شیمیایی نمایشی از عناصر شیمیایی است که براساس ساختار الکترونی مرتب شده است، بطوریکه بسیاری از خواص شیمیایی بصورت منظم در طول جدول تغییر نماید. جدول اولیه بدون اطلاع از ساختار داخلی اتمها ساخته شد: اگر عناصر را بر حسب جرم اتمی آنها مرتب نمائیم، و آنگاه نمودار خواص معین دیگر آنها را بر حسب جرم اتمی رسم نمائیم، میتوان نوسان یا تناوب این خواص را بصورت تابعی از جرم اتمی مشاهده نمود. اولین کسی که توانست این نظم را مشاهده نماید، یک شیمیدان آلمانی به نام Johann Wolfgang D?einer بود. او متوجه تعدادی تثلیث از عناصر مشابه شد:
نمونه تثلیث ها
عنصر جرم اتمی چگالی ------ عنصر جرم اتمی چگالی
Cl 35.5 1.56 g/L ------ Ca 40.1 1.55 g/cm3
Br 79.9 3.12 g/L ------ Sr 87.6 2.6 g/cm3
I 126.9 4.95 g/L ------ Ba 137 3.5 g/cm3
و به دنبال او، شیمیدان انگلیسی John Alexander Reina Newlands متوجه گردید که عناصر از نوع مشابه در فاصلههای هشت تایی یافت می شوند، که آنها را با نتهای هشتگانه موسیقی شبیه نمود، هرچند که قانون نتهای او مورد تمسخر معاصرین او قرار گرفت. سرانجام شیمیدان آلمانی Lothar Meyer و شیمیدان روسی Dmitry Ivanovich Mendeleev تقریبا بطور همزمان اولین جدول تناوبی را، با مرتب نمودن عناصر بر حسب جرمشان، توسعه دادند( ولی مندلیف تعداد کمی از عناصر را خارج از ترتیب صریح جرمی، برای تطابق بهتر با خواص همسایگانشان رسم نمود – این کار بعدها با کشف ساختار الکترونی عناصر در اواخر قرن نوزدهم و اوایل قرن بیستم توجیه گردید). فهرست عناصر بر اساس نام، علامت اختصاری و عدد اتمی موجود میباشد. شکل زیر جدول تناوبی عناصر شناخته شده را نمایش میدهد. هر عنصر با عدد اتمی و علامتهای شیمیایی. عناصر در یک ستون ("گروه") از لحاظ شیمیایی مشابه می باشند.
| http://www.www.www.iran-eng.ir/images/statusicon/wol_error.gif | این عکس کوچک شده است، برای اینکه بصورت بزرگ شده ببینید، روی این قسمت کلیک کنید، اندازه اصلی عکس 454x742 و حجم آن 105 می باشد. |

کد رنگ برای اعداد اتمی:
عناصر شماره گذاری شده با رنگ آبی ، در دمای اتاق مایع هستند؛
عناصر شماره گذاری شده با رنگ سبز ، در دمای اتاق بصورت گاز می باشند؛
عناصر شماره گذاری شده با رنگ سیاه، در دمای اتاق جامد هستند.
عناصر شماره گذاری شده با رنگ قرمز ترکیبی بوده و بطور طبیعی یافت نمی شوند(همه در دمای اتاق جامد هستند.)
عناصر شماره گذاری شده با رنگ خاکستری ، هنوز کشف نشدهاند (و بصورت کم رنگ نشان داده شدهاند تا گروه شیمیایی را که در آن قرار می گیرند، مشخص نماید.(
و می توانید دراین کلید واژه جدول برای تشدید مغناطیسی را بیابید.
تعداد لایه الکترون در یک اتم تعیین کننده ردیفی است که در آن قرار می گیرد. هر لایه به زیرلایه های متفاوتی تقسیم میشود، که هر اندازه عدد اتمی افزایش می یابد، این لایه ها به ترتیب زیر:
1s
2s 2p
3s 3p
4s 3d 4p
5s 4d 5p
6s 4f 5d 6p
7s 5f 6d 7p
8s 5g 6f 7d 8p
...
براساس ساختار جدول پر میشوند. از آنجائیکه الکترونهای خارجی ترین لایه، خواص شیمیایی را تعیین مینمایند، این لایه ها در میان گروهای یکسان مشابه اند.عناصر همجوار با یکدیگر در یک گروه، علیرغم اختلاف مهم در جرم، دارای خواص فیزیکی مشابه میباشند. عناصر همجوار با یکدیگر در یک ردیف دارای جرم های مشابه ولی خواص متفاوت میباشند.
برای مثال، عناصر بسیار نزدیک به نیتروژن (N) در ردیف دوم کربن© و اکسیژن(O) میباشند. علیرغم تشابه آنها در جرم ( که بصورت ناچیزی در واحد جرم اتمی تفاوت دارند)، دارای خواص بینهایت متفاوتی هستند، همانطور که با بررسی فرمهای دیگر میتوان ملاحظه نمود: اکسیژن دو اتمی یک کاز است که سوختن را تشدید می نماید، نیتروژن دو اتمی یک گاز است که سوختن را تشدید نمی کند، و کربن یک جامد است که میتواند سوزانده شود( بله، میتوان الماس را سوزاند!).
در مقایسه، عناصر بسیار نزدیک به کلر (Cl) در گروه یکی مانده به آخر در جدول «هالوژنها) فلوئور( F) و برم( Br) میباشند. علیرغم تفاوت فاحش جرم آنها در گروه، فرمهای دیگر آنها دارای خواص بسیار مشابه میباشند: آنها بسیار خورنده ( بدین معنی که تمایل خوبی برای ترکیب با فلزات، برای تشکیل نمک هالاید فلز)؛ کلر و فلوئور گاز هستند، درحالیکه برم یک مایع با تبخیر بسیار کم میباشد؛ کلر و برم بسیار رنگی هستند
xpersia
عضو جدید
termah
مدیر بازنشسته
جملاتی برای حفظ جدول تناوبی
جملاتی برای حفظ جدول تناوبی
[h=2] جمله هایی برای حفظ جدول تناوبی
[/h]
جمله هایی برای حفظ جدول تناوبی
گروه I A : لینا کارخونه ی رب سازی فرانسه!!! (Li-Na-K-Rb-Cs-Fr)
گروه II A : بگو مجید کلتو سوراخ می کنم با رنده!!! (Be-Mg-Ca-Sr-Ba-Ra)
گروه III A : بگو الو جواد این جا تالاره؟؟؟!!! (B-Al-Ga-In-Tl)
گروه IV A : کسی ژله ی سنگ و پنبه دیده؟؟؟ (C-Si-Ge-Sn-Pb)
گروه V A : نگو پلو از(س) سوب بِیتِره(به زبان اصفهانی میشه بهتره!!!!)!!! (N-P-As-Sb-Bi)
گروه VI A : استاد سه تا تریلی پکوند!!! (O-S-Se-Te-Po)
گروه VII A : فُکُلی بریم آتن!!! (F-Cl-Br-I-At)
گروه VIII A : هِی نِکبَت (ببخشید... ) ارّه کردی زنبیل رعنا رو!!!! (He-Ne-Ar-Kr-Xe-Rn)
و سطر اول عناصر واسطه: اِسکاتی، وِل کن کره ی منو، فِرار کنی، سوزوندمت...ش
جملاتی برای حفظ جدول تناوبی
[h=2] جمله هایی برای حفظ جدول تناوبی
[/h]
جمله هایی برای حفظ جدول تناوبی
گروه I A : لینا کارخونه ی رب سازی فرانسه!!! (Li-Na-K-Rb-Cs-Fr)
گروه II A : بگو مجید کلتو سوراخ می کنم با رنده!!! (Be-Mg-Ca-Sr-Ba-Ra)
گروه III A : بگو الو جواد این جا تالاره؟؟؟!!! (B-Al-Ga-In-Tl)
گروه IV A : کسی ژله ی سنگ و پنبه دیده؟؟؟ (C-Si-Ge-Sn-Pb)
گروه V A : نگو پلو از(س) سوب بِیتِره(به زبان اصفهانی میشه بهتره!!!!)!!! (N-P-As-Sb-Bi)
گروه VI A : استاد سه تا تریلی پکوند!!! (O-S-Se-Te-Po)
گروه VII A : فُکُلی بریم آتن!!! (F-Cl-Br-I-At)
گروه VIII A : هِی نِکبَت (ببخشید... ) ارّه کردی زنبیل رعنا رو!!!! (He-Ne-Ar-Kr-Xe-Rn)
و سطر اول عناصر واسطه: اِسکاتی، وِل کن کره ی منو، فِرار کنی، سوزوندمت...ش
کامل ترین جدول تناوبی
کامل ترین جدول تناوبی
باکلیک بر روی لینک زیر به یک جدول تناوبی فوق العاده خواهید رسید که علاوه بر اطلاعات معمولی مانند نماد و نام عنصر عدد اتمی و عدد جرمی و........که هر جدول تناوبی می دهد اطلاعات زیر را در اختیار شما قرار می دهد:
1-آرایش لایه ای هر عنصر
2- دسته بندی کامل عناصر
3- با کلیک بر روی خواص و سپس نماد هر عنصر به اطلاعات کاملی ازجمله حالت فیزیکی ،دمای ذوب ، دمای جوش، انرژی یونش ، قدرت الکترونگاتیوی ، انرژی الکترون خواهی ، ظرفیت ، شعاع یونی ، درصد فر اونی ، سال کشف ، چگالی و........
4-با کلیک بر روی compound و سپس بر روی هر عنصر متداول ترین ترکیبات عنصر مورد نظر را خواهید دید
5- با کلیک بر روی ایزوتوپ و سپس بر روی هر عنصر کلیه ایزوتوپ های عنصر مورد نظررا خواهید دید که اگر نمایشگر ماوس را بر روی هر ایزوتوپ برید خواص ایزوتوپ فهرست خواهد شد
6- با کلیک بر روی اوربیتال و سپس نماد هر عنصر آرایش کلیه اوربیتالهای پر شده عنصر نمایش داده خواهد شد
برای دریافت جدول اینجا را کلیک کنید
کامل ترین جدول تناوبی
باکلیک بر روی لینک زیر به یک جدول تناوبی فوق العاده خواهید رسید که علاوه بر اطلاعات معمولی مانند نماد و نام عنصر عدد اتمی و عدد جرمی و........که هر جدول تناوبی می دهد اطلاعات زیر را در اختیار شما قرار می دهد:
1-آرایش لایه ای هر عنصر
2- دسته بندی کامل عناصر
3- با کلیک بر روی خواص و سپس نماد هر عنصر به اطلاعات کاملی ازجمله حالت فیزیکی ،دمای ذوب ، دمای جوش، انرژی یونش ، قدرت الکترونگاتیوی ، انرژی الکترون خواهی ، ظرفیت ، شعاع یونی ، درصد فر اونی ، سال کشف ، چگالی و........
4-با کلیک بر روی compound و سپس بر روی هر عنصر متداول ترین ترکیبات عنصر مورد نظر را خواهید دید
5- با کلیک بر روی ایزوتوپ و سپس بر روی هر عنصر کلیه ایزوتوپ های عنصر مورد نظررا خواهید دید که اگر نمایشگر ماوس را بر روی هر ایزوتوپ برید خواص ایزوتوپ فهرست خواهد شد
6- با کلیک بر روی اوربیتال و سپس نماد هر عنصر آرایش کلیه اوربیتالهای پر شده عنصر نمایش داده خواهد شد
برای دریافت جدول اینجا را کلیک کنید
arash_1376
کاربر فعال
Similar threads
| Thread starter | عنوان | تالار | پاسخ ها | تاریخ |
|---|---|---|---|---|
| ح | آزمایشی برای ترکیب همه عناصر جدول تناوبی! | شیمی معدنی | 0 |





