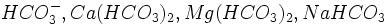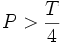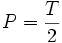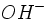termah
مدیر بازنشسته
اسیدیته آب
دیاکسید کربن در محلولهای آبی به صورت آزاد یا به شکل یونهای کربناتی یا بیکربناتی وجود دارد. وجود این گاز در آب میتواند ناشی از حل شدن
 موجود در هوا و یا تجزیه مواد آلی موجود در آب باشد، با وجودیکه مقدار
موجود در هوا و یا تجزیه مواد آلی موجود در آب باشد، با وجودیکه مقدار
 موجود در هوا کمتر از حدود 0.04 درصد است، ولی این مقدار در آبهای سطحی در مقایسه با اکسیژن محلول قابل توجه بوده و به 10ppm میرسد. در آب چاهها این مقدار تا حد 100ppm میرسد.
موجود در هوا کمتر از حدود 0.04 درصد است، ولی این مقدار در آبهای سطحی در مقایسه با اکسیژن محلول قابل توجه بوده و به 10ppm میرسد. در آب چاهها این مقدار تا حد 100ppm میرسد.

تأثیر
 محلول در آب در تأسیسات صنعتی
محلول در آب در تأسیسات صنعتی
خورندگی یکی از تأثیرات مهم
 محلول در آب است،
محلول در آب است،
 در آب تبدیل به اسید کربنیک میشود که ترکیبی خورنده است. مخصوصاً در PHهای پائین علاوه بر اینکه اسید کربنیک خورنده تولید میشود، خاصیت خورندگی اکسیژن هم بالا میرود. از اینروست که باید
در آب تبدیل به اسید کربنیک میشود که ترکیبی خورنده است. مخصوصاً در PHهای پائین علاوه بر اینکه اسید کربنیک خورنده تولید میشود، خاصیت خورندگی اکسیژن هم بالا میرود. از اینروست که باید
 موجود در آب خارج شود.
موجود در آب خارج شود.
در جوشآورها ، خورندگی ناشی از
 اغلب در مسیر بخار داغ و خط آب مقطر برگشتی دیده میشود و این
اغلب در مسیر بخار داغ و خط آب مقطر برگشتی دیده میشود و این
 ناشی از تجزیه کربناتها و بیکربناتها در شرایط داخلی جوشآورها میباشد. هیدروکسید سدیم ، محصول جانبی این واکنشها میباشد. خورندگی بخار آب داغ و آب مقطر برگشتی اغلب در جوشآورهایی که آب مصرف شده در آنها دارای قلیائیت متیل اورانژ بالایی هستند بیشتر دیده میشود.
ناشی از تجزیه کربناتها و بیکربناتها در شرایط داخلی جوشآورها میباشد. هیدروکسید سدیم ، محصول جانبی این واکنشها میباشد. خورندگی بخار آب داغ و آب مقطر برگشتی اغلب در جوشآورهایی که آب مصرف شده در آنها دارای قلیائیت متیل اورانژ بالایی هستند بیشتر دیده میشود.
در این نوع جوشآورها مقدار تقریبی
 در بخار داغ را میتوان با ضرب قلیائیت متیل اورانژ آب تغذیه به جوشآورها عدد و 0.7 بدست آورد و این بمعنی تجزیه 80% کربنات سدیم میباشد. یعنی اگر قلیائیت متیل اورانژ آب تغذیه به جوشآورها 100ppm باشد باید انتظار داشت که مقدار
در بخار داغ را میتوان با ضرب قلیائیت متیل اورانژ آب تغذیه به جوشآورها عدد و 0.7 بدست آورد و این بمعنی تجزیه 80% کربنات سدیم میباشد. یعنی اگر قلیائیت متیل اورانژ آب تغذیه به جوشآورها 100ppm باشد باید انتظار داشت که مقدار
 در بخار داغ 79ppm باشد که این مقدار
در بخار داغ 79ppm باشد که این مقدار
 بشدت خورنده است.
بشدت خورنده است.
روش اندازه گیری
روش تیتراسیون مستقیم در محدوده 100ppm قابل استفاده است. در این روش
 آزاد با محلول کربنات سدیم و یا یک محلول قلیایی دیگر ترکیب و تولید بیکربنات خواهد کرد. پس از ترکیب کلیه
آزاد با محلول کربنات سدیم و یا یک محلول قلیایی دیگر ترکیب و تولید بیکربنات خواهد کرد. پس از ترکیب کلیه
 ، بیکربنات اضافی در محیط باقی خواهد ماند. در این شرایط که PH برابر 8.3 است. رنگ صورتی شناساگر فنل فتالین ظاهر خواهد شد.
، بیکربنات اضافی در محیط باقی خواهد ماند. در این شرایط که PH برابر 8.3 است. رنگ صورتی شناساگر فنل فتالین ظاهر خواهد شد.
اگر بلافاصله بعد از اضافه کردن معرف به ظرف حاوی نمونه آب ، رنگ قرمز ظاهر شود میتوان نتیجه گرفت که
 در نمونه وجود ندارد. اما اگر نمونه بیرنگ ماند، با کربنات سدیم تیتر میشود تا رنگ صورتی با پایداری 30 ثانیه حاصل شود.
در نمونه وجود ندارد. اما اگر نمونه بیرنگ ماند، با کربنات سدیم تیتر میشود تا رنگ صورتی با پایداری 30 ثانیه حاصل شود.
عوامل مداخله کننده
وجود اسیدهای معدنی ، فلزات سنگین و مقدار زیاد مواد محلول در آب از عوامل مؤثر در اندازه گیری و نتایج هستند. طریقه نمونه برداری هم از عوامل مهم
دیاکسید کربن در محلولهای آبی به صورت آزاد یا به شکل یونهای کربناتی یا بیکربناتی وجود دارد. وجود این گاز در آب میتواند ناشی از حل شدن



تأثیر

خورندگی یکی از تأثیرات مهم



در جوشآورها ، خورندگی ناشی از


در این نوع جوشآورها مقدار تقریبی



روش اندازه گیری
روش تیتراسیون مستقیم در محدوده 100ppm قابل استفاده است. در این روش


اگر بلافاصله بعد از اضافه کردن معرف به ظرف حاوی نمونه آب ، رنگ قرمز ظاهر شود میتوان نتیجه گرفت که

عوامل مداخله کننده
وجود اسیدهای معدنی ، فلزات سنگین و مقدار زیاد مواد محلول در آب از عوامل مؤثر در اندازه گیری و نتایج هستند. طریقه نمونه برداری هم از عوامل مهم